Содержание
Это крупнейший прорыв за последние 20 лет в области кроветворения, который дает надежду на лечение лейкоза и других тяжелых болезней крови.
Команда из Базельского университета и университетской клиники Базеля (Швейцария) впервые в мире создала полностью человеческую ткань костного мозга, которая не просто лежит в чашке, а живет и производит клетки крови несколько недель подряд. Это не фантастика и не упрощенная модель — это настоящая трехмерная «мини-кость» со всеми нужными отсеками и правильными соседями клеток. Результаты работы были опубликованы в журнале Cell.
Почему старые методы больше не подходят
Костный мозг представляет собой не просто мягкую ткань внутри костей, а высокоорганизованную биологическую систему, где ежедневно формируется порядка полутриллиона клеток крови. Кроветворение происходит в специализированных микросредах — нишах, в которых стволовые клетки взаимодействуют с костными клетками, кровеносными сосудами, нервными окончаниями и стромальными структурами. Особое значение имеет эндостальная ниша — тонкая зона у внутренней поверхности кости. Именно в этом участке лейкозные клетки могут сохраняться в скрытом состоянии и приобретать устойчивость к химиотерапевтическому лечению.
До сих пор изучать это можно было только на мышах (у них ниша устроена иначе) или в плоских культурах (клетки теряют свои свойства уже через 48 часов). Ни один из этих подходов не давал точной картины того, что происходит в человеческом организме.
Как именно сделали работающую «фабрику»
Все началось с индуцированных плюрипотентных стволовых клеток (iPSC), полученных из кожи или крови обычных доноров. Их поместили в пористый каркас из гидроксиапатита и коллагена первого типа — материал почти идентичный настоящей кости. Каркас размером 8 мм в диаметре и 4 мм толщиной напоминает маленькую губку с миллионами микропор и каналов.
Затем начался сложный процесс корректировки. Сначала добавляли фактор роста VEGF и BMP-2 — клетки превращались в эндотелий и выстилали будущие сосуды. Потом шел коктейль из TGF-β и дексаметазона — появлялись остеобласты, которые начинали откладывать минерал и укреплять каркас. На третьем этапе подключили SCF, TPO и IL-3 — и в ниши заселялись кроветворные стволовые клетки CD34+. Через 25–30 дней внутри этой искусственной кости сформировалась полноценная эндостальная ниша, а кроветворение запустилось само собой.
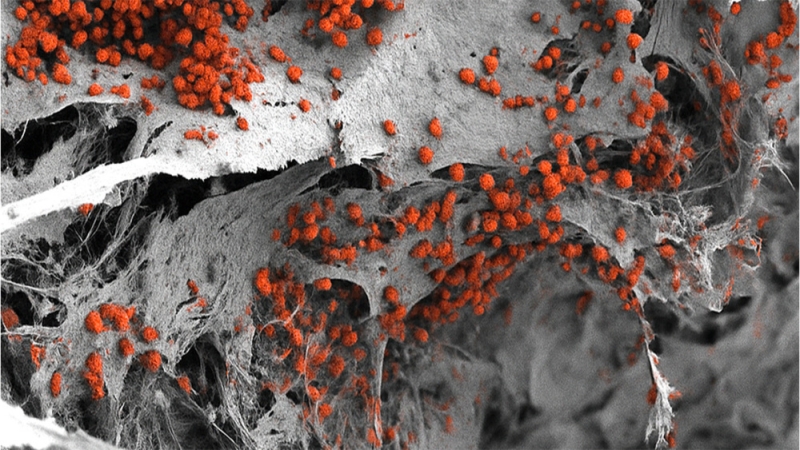
Под сканирующим электронным микроскопом видно, как эритроциты и гранулоциты выходят из ниш и плавают в искусственных сосудах. Ткань живет минимум четыре недели и все это время выдает новые клетки крови — примерно как настоящий костный мозг в бедре взрослого человека.
Что это дает прямо сейчас
Во-первых, ученые наконец могут изучать человеческий лейкоз на человеческих же клетках в правильной трехмерной среде.
Во-вторых, появилась возможность тестировать лекарства так, как это происходит в реальном организме.
В-третьих, уже через пару лет врачи смогут брать клетки конкретного пациента, выращивать его личный костный мозг и за неделю понять, какое лечение сработает лучше всего.
«Это может послужить дополнением ко многим экспериментам на животных по изучению кроветворения как в здоровых, так и в больных условиях», — говорит руководитель проекта профессор Иван Мартин.
Что еще предстоит доделать
Пока образец довольно большой — 8 мм. Для массового скрининга лекарств нужно уменьшить его в 5–10 раз. Команда уже работает над чипами, где на одном стекле будет сразу 96 или 384 мини-кости. Еще одна задача — продлить жизнь ткани до 3–4 месяцев, чтобы можно было моделировать хронические болезни.
Но даже в нынешнем виде это крупнейший прорыв за последние 20 лет в области кроветворения. Впервые ученые получили инструмент, который позволяет изучать заболевания крови непосредственно в условиях, максимально приближенных к человеческой физиологии, а не опираться главным образом на модели мышей. Это дает реальную надежду, что в течение ближайших 5–7 лет потребность в животных экспериментах при исследовании лейкозов и миелодиспластических синдромов значительно сократится.